摘要
2021年8月26日美國(guó)化學(xué)會(ACS)期刊NANO發表了國(guó)家納米中(zhōng)心聶廣軍、王海課題組與北京中(zhōng)醫(yī)藥大學(xué)東方醫(yī)院李慧課題組最新(xīn)的研究成果。論文(wén)的題目是“Separable Microneedle Patch toProtect and Deliver DNA Nanovaccines Against COVID-19”。
這是一篇将DNA新(xīn)冠疫苗做成可(kě)溶解微針的最新(xīn)研究成果,與當前肆虐全球的新(xīn)冠疫情緊密相關。青瀾生物(wù)作(zuò)為(wèi)可(kě)溶解微針技(jì )術産(chǎn)業化的先行者,我們認為(wèi)這是一篇不可(kě)多(duō)得的高水平研究文(wén)獻,下面青瀾就和大家一起詳細解讀這篇文(wén)獻,并結合公(gōng)司自己的微針疫苗研發實踐,一同認識可(kě)溶解微針DNA疫苗技(jì )術。
一、DNA疫苗與可(kě)溶解微針技(jì )術相結合,取得了較好的免疫效果
在2020年初我國(guó)國(guó)家科(kē)技(jì )部确定的五條疫苗技(jì )術路線(xiàn)中(zhōng),基因疫苗代表最新(xīn)的技(jì )術路線(xiàn)。在新(xīn)冠疫情來臨之前,全球尚無一款人用(yòng)的基因疫苗上市,基因疫苗的新(xīn)穎性可(kě)見一斑。基因疫苗又(yòu)分(fēn)為(wèi)mRNA疫苗和DNA疫苗,2020年12月21日輝瑞/BioNtech的mRNA新(xīn)冠疫苗在歐盟有(yǒu)條件獲批上市,這是曆史上首個上市用(yòng)于人體(tǐ)的mRNA疫苗。 DNA疫苗是将抗原蛋白編碼的DNA片段通過生物(wù)工(gōng)程大量表達出來,做成具(jù)備各種功能(néng)段的環狀DNA質(zhì)粒。DNA質(zhì)粒被遞送進入細胞核内轉錄為(wèi)RNA,再由後者翻譯成抗原蛋白。基因疫苗相當于把抗原的生産(chǎn)過程從醫(yī)藥車(chē)間搬到細胞内,基因疫苗能(néng)夠同時激起機體(tǐ)的體(tǐ)液免疫和細胞免疫。美國(guó)NASDAQ上市公(gōng)司Inovio Pharmaceuticals, Inc.和港股準上市公(gōng)司蘇州艾棣維欣是全球DNA疫苗研發的佼佼者,目前兩家合作(zuò)的DNA新(xīn)冠疫苗正在全球9個國(guó)家開展三期臨床試驗。
2021年8月20日,印度藥物(wù)監管機構批準使用(yòng)DNA新(xīn)冠肺炎疫苗ZyCoV-D,在近日的臨床試驗中(zhōng),該款三劑式的疫苗有(yǒu)效率達66%,成為(wèi)印度第二種獲得批準的國(guó)産(chǎn)疫苗。這也是世界上第一種新(xīn)冠病毒DNA疫苗。有(yǒu)科(kē)技(jì )媒體(tǐ)調研發現,印度獲批的DNA疫苗在序列設計上與艾棣維欣/INOVIO已經發表的臨床前研究披露的序列設計高度一緻,但是考慮到印度疫情的嚴重程度,目前未有(yǒu)看到任何一方有(yǒu)相應的知識産(chǎn)權方面的訴求。
聶廣軍課題組等将最新(xīn)的DNA疫苗與概念性十足的可(kě)溶解微針技(jì )術結合,在體(tǐ)外試驗和動物(wù)試驗中(zhōng)都取得了較好的免疫效果。如果可(kě)以産(chǎn)業化,将真正地實現“不打針不吃藥”即完成疫苗的接種,突破現有(yǒu)技(jì )術,實現新(xīn)的突破。
(圖1)
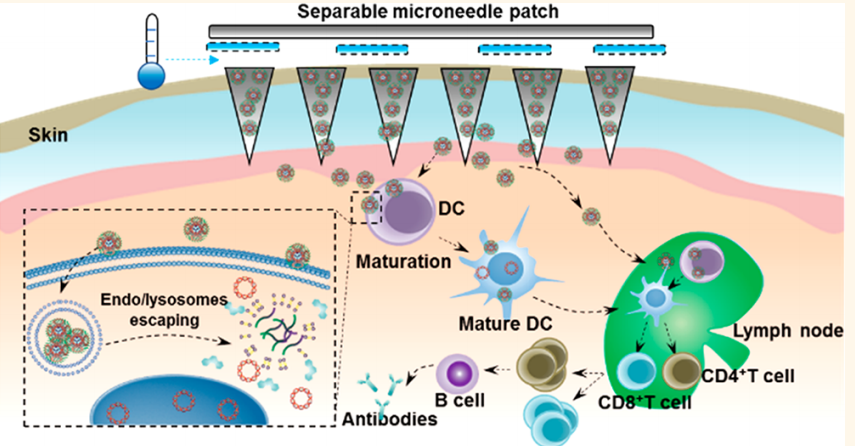
如圖1所示,研究者設計的微針貼由三部分(fēn)構成,分(fēn)别是載有(yǒu)DNA質(zhì)粒的針體(tǐ)部分(fēn),由溫敏材料組成的藍色中(zhōng)間分(fēn)離層以及用(yòng)于承載微針的灰色基膜層。當載有(yǒu)疫苗的微針貼在皮膚上以後,降低溫度,藍色的分(fēn)離層會逐漸液化(在14攝氏度左右,藍色中(zhōng)間分(fēn)離層會液化從而使針體(tǐ)斷裂并留在皮膚内),揭掉基膜,即可(kě)實現疫苗的接種,設計概念非常巧妙。由于表皮層是抗原呈遞細胞(APC,圖1中(zhōng)DC即是APC的一種)最豐富的部位,因此也是最好的免疫部位,比肌肉注射更少的疫苗劑量即可(kě)實現同等的免疫應答(dá)。
二、微針DNA新(xīn)冠疫苗貼的邏輯和技(jì )術難度
根據DNA疫苗的起效原理(lǐ),隻有(yǒu)将DNA疫苗遞送進入細胞核才可(kě)以發揮作(zuò)用(yòng)。如何将DNA疫苗成功遞送到細胞核内,是該類疫苗成功研發的關鍵。微針刺破角質(zhì)層,将DNA疫苗成功遞送到皮膚的組織液,接下來還需要透過細胞膜,完成細胞質(zhì)中(zhōng)的溶酶體(tǐ)逃逸,穿過細胞核膜才可(kě)以到達細胞核。由于機制複雜,基因藥物(wù)的遞送在高校的藥劑學(xué)教材中(zhōng),都是作(zuò)為(wèi)難度較大藥物(wù)劑型放在最後介紹。
此外,聶廣軍課題組還将R848作(zuò)為(wèi)DNA疫苗的佐劑,與DNA疫苗進行同步遞送。由于R848這個佐劑不溶于水,要想成功完成DNA疫苗的遞送并發生效力,需要解決的技(jì )術難點多(duō)且大。
(圖2)
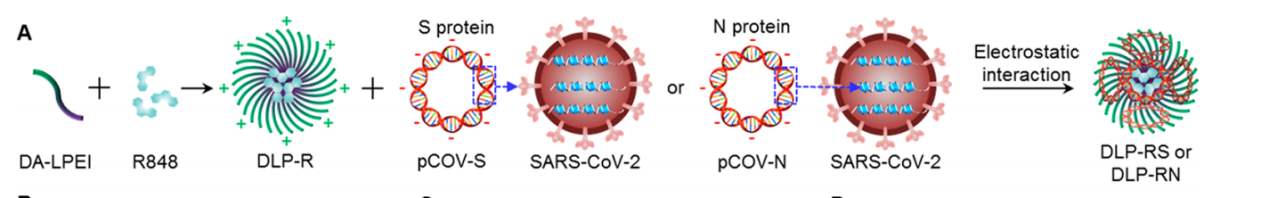
為(wèi)了完成上述目标,聶廣軍課題組等巧妙的進行了藥物(wù)載體(tǐ)設計,如圖2所示,采用(yòng)了PEI納米顆粒,PEI是陽離子聚合物(wù),表面帶有(yǒu)大量正電(diàn)荷,内部疏水基團剛好用(yòng)于包裹油溶性的R848佐劑。
PEI納米顆粒外面可(kě)以吸附帶負電(diàn)的DNA質(zhì)粒。PEI納米顆粒攜帶了DNA質(zhì)粒和佐劑,能(néng)夠完成透過細胞膜,良好的溶酶體(tǐ)逃逸能(néng)力,能(néng)最終将DNA質(zhì)粒和佐劑成功遞送進入細胞核内。圖2方法制得的DNA納米粒子溶液與PVA材料組成了圖1所示的針體(tǐ)部分(fēn),在皮膚上貼敷後,針體(tǐ)部分(fēn)溶斷在皮膚内。包含DNA質(zhì)粒的納米顆粒經過細胞的内吞作(zuò)用(yòng),被APC捕獲,研究者通過一系列的染色試驗,證明了納米顆粒被細胞成功内吞、轉染以及抗原S和N蛋白的表達。作(zuò)者甚至通過分(fēn)離提純,在WESTERN POINT裏宏觀看到了所表達的S和N蛋白。整個試驗設計邏輯嚴謹,試驗結果充分(fēn),間接和直接的證據都表明,微針DNA新(xīn)冠疫苗貼能(néng)夠在體(tǐ)内成功的實現了免疫。
接下來,我們再通過圖3觀察一下微針疫苗貼的貼敷過程和貼前貼後微針貼的完整顯微照片。
(圖3)
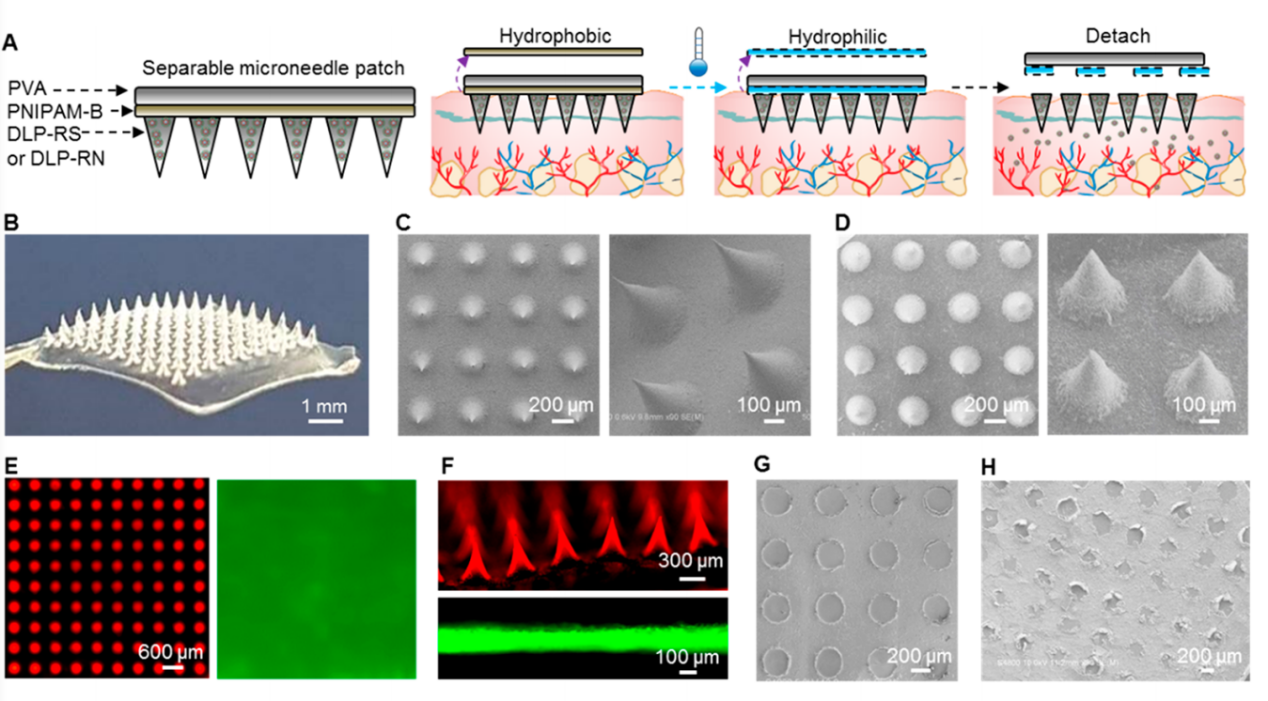
我們可(kě)以看到,貼敷後的殘貼上可(kě)以清晰的看到針體(tǐ)斷裂後留下的空位。當把載有(yǒu)DNA質(zhì)粒的針尖液進行紅色染料标記時,通過俯視圖和平視圖,可(kě)以清晰的看到針體(tǐ)部分(fēn)完整無缺失。
微針和性質(zhì)穩定的DNA疫苗技(jì )術結合,做成DNA疫苗微針貼,不需要注射器,徒手就可(kě)以貼敷,貼敷過程猶如使用(yòng)創可(kě)貼,而且患者無痛感,極大地提升了患者在接種疫苗的依從性。
為(wèi)了驗證常溫下DNA疫苗微針貼的穩定性,研究者做了在室溫下的儲存試驗。結果表明,室溫放置幾個月的DNA疫苗微針貼,依然能(néng)夠具(jù)有(yǒu)充足的免疫原性。也就是說,DNA疫苗微針貼不需要冷鏈保存和運輸——這對于發展水平低下的國(guó)家和地區(qū)具(jù)有(yǒu)非常重要的現實意義,極大的提升了疫苗在這些地區(qū)的可(kě)及性。這不僅僅是核酸疫苗開發重大進展,也是整個疫苗領域重大的技(jì )術性突破。
此外,作(zuò)為(wèi)平行試驗組,研究者還做了沒有(yǒu)PEI納米粒子包裹的裸DNA質(zhì)粒的微針貼,結果沒有(yǒu)觀察到細胞轉染,也沒有(yǒu)得到最終的S和N抗原蛋白的表達。研究者認為(wèi)這體(tǐ)現了PEI納米顆粒體(tǐ)系對于DNA質(zhì)粒遞送的重要性和必要性。
文(wén)章有(yǒu)提到PEI雖然廣泛的被用(yòng)于基因藥物(wù)的遞送,但是它的細胞毒性是潛在應用(yòng)存在的一個嚴肅問題。研究者認為(wèi)降低PEI的分(fēn)子量會降低它的毒性,但是并不能(néng)完全消除它的細胞毒性。青瀾生物(wù)注意到在由潘衛三教授主編的全國(guó)高等教育藥學(xué)類規劃教材《藥劑學(xué)》的基因藥物(wù)遞送章節中(zhōng),也提到了非病毒載體(tǐ)的PEI材料,PEI包裹的DNA質(zhì)粒具(jù)有(yǒu)良好的透過細胞膜和溶酶體(tǐ)逃逸能(néng)力。PEI被廣泛地用(yòng)于研究型的細胞轉染實驗,但是目前尚無含有(yǒu)PEI材料的藥物(wù)産(chǎn)品得到監管部門的批準。
青瀾生物(wù)于2021年2月開始與蘇州艾棣維欣合作(zuò)進行DNA新(xīn)冠微針貼疫苗的開發,雙方的目标是該技(jì )術成功的産(chǎn)業化,将産(chǎn)品最終推向市場。
微針概念的提出有(yǒu)幾十年了,可(kě)溶解微針技(jì )術的提出也有(yǒu)近20年的曆史,我們經常說微針技(jì )術是平台技(jì )術,可(kě)以廣泛的用(yòng)于藥物(wù)的遞送。然而,當我們具(jù)體(tǐ)開展某款藥物(wù)的微針劑型時,依然是“從0到1”的過程,需要解決的技(jì )術問題非常多(duō),難度也非常大。這也是為(wèi)什麽微針技(jì )術的發展前景被非常看好、但至今卻仍未在藥物(wù)遞送領域真正走向商(shāng)品化的原因。
綜上我們所解讀的文(wén)獻研究内容,我們了解到上述研究遞送的目标藥物(wù)與青瀾生物(wù)所遞送的目标藥物(wù)完全一緻,這體(tǐ)現了青瀾生物(wù)在DNA微針疫苗研究領域的前沿性,同時對我們的産(chǎn)業化研究也有(yǒu)深度的啓發。《NANO》是ACS的知名(míng)期刊,影響因子(IF)超過17,是國(guó)際頂級期刊。在《NANO》上剛剛發表的這項前瞻性研究屬于基礎研究,橫跨了DNA疫苗和可(kě)溶解微針兩大前沿技(jì )術,但是要想實現這項技(jì )術的商(shāng)業化往往是論文(wén)發表後若幹年的事情。這還不是困難的全部,疫苗的研發和推向市場在解決技(jì )術問題的同時,還要滿足監管部門的法規要求。
不過好在微針技(jì )術是一個結果導向的技(jì )術,不管過程有(yǒu)多(duō)複雜難度有(yǒu)多(duō)大,它的終極目的是為(wèi)了實現藥物(wù)遞送,讓藥物(wù)發揮作(zuò)用(yòng)。不過,在做這個技(jì )術研發的過程中(zhōng),還要同步滿足藥監部門的法規要求。青瀾生物(wù)和艾棣維欣都是商(shāng)業化的企業,無論面對的項目有(yǒu)多(duō)難,雙方在決策啓動項目之前,目标非常明确,就是盡快實現微針藥物(wù)遞送的産(chǎn)業化。
三、青瀾關于微針疫苗的4點思考
由于青瀾生物(wù)和艾棣維欣的相關研究尚未發表,因此很(hěn)多(duō)數據和結果尚不能(néng)在此公(gōng)開。青瀾的微針研發部分(fēn)我們隻能(néng)以點帶面,把一些研究結果與大家分(fēn)享,過程涉及技(jì )術秘密,暫時不深入讨論。
在此我們僅就四個問題點進行讨論,但是并不意味着我們需要解決的問題隻有(yǒu)這四個方面。
一、接種時間
衆所周知,常規注射疫苗在接種後,需要在留置點觀察30分(fēn)鍾,如有(yǒu)意外情況便于醫(yī)務(wù)人員及時處置。将疫苗接種方式改為(wèi)可(kě)溶解微針貼以後,如果我們要求接種者留置數個小(xiǎo)時,那肯定不能(néng)被患者接受,集中(zhōng)接種點也無法容納那麽多(duō)的接種者。因此,我們必須把接種時間和留置觀察的總時間作(zuò)為(wèi)微針疫苗的研發輸入條件。
接種時間要與傳統肌注相當,再留置觀察30分(fēn)鍾。為(wèi)此聶廣軍課題組的文(wén)章中(zhōng)将微針貼設計成了三層結構,中(zhōng)間的分(fēn)離層能(néng)很(hěn)快地液化從而讓針體(tǐ)部分(fēn)實現快速斷裂。但是研究者選用(yòng)的快速分(fēn)離材料要求的溫度是14-16攝氏度(詳細見論文(wén)相應部分(fēn)),這個要求在疫苗接種實踐中(zhōng)顯然難以實現,這個設計也導緻微針成品的質(zhì)量容易受到溫度的影響。從實驗室研究的角度來看,采用(yòng)這樣的技(jì )術方案無可(kě)厚非,能(néng)達到最終的研究目的即可(kě)。但如果最終目的是需要上市申報的微針疫苗貼,必須采用(yòng)可(kě)靠的工(gōng)藝和合法合規的材料來實現,使用(yòng)任何不被藥典收錄的材料,都将會給藥品申報帶來巨大的法規方面的困難。
青瀾生物(wù)采用(yòng)專利技(jì )術,完全使用(yòng)藥典内材料,隻需幾秒(miǎo)的貼敷時間,即可(kě)實現微針藥物(wù)在皮内快速釋放,幾乎是貼上即可(kě)移除。具(jù)體(tǐ)參見視頻展示。我們能(néng)夠看到貼敷之前顯微鏡可(kě)見染色針體(tǐ)整齊排列無缺損,貼敷好以後立即揭掉,我們看到揭下來的殘貼上染色針尖都不見了(此處我們以同樣具(jù)有(yǒu)角質(zhì)層的樹葉來代替皮膚)。在顯微鏡下觀察樹葉表面,發現每個刺入孔内都有(yǒu)染色的藥物(wù)。

二、工(gōng)藝問題
從圖3可(kě)以看到,聶廣軍課題組團隊開發的微針由三層材料構成,這也就意味着微針的生産(chǎn)過程會使用(yòng)三種溶液進行制膜,所使用(yòng)的材料是否滿足法規要求不談,這樣的工(gōng)藝會導緻生産(chǎn)效率較為(wèi)低下,藥品質(zhì)量控制難度大,生産(chǎn)過程中(zhōng)和後續物(wù)流存儲過程藥品質(zhì)量風險大。 從視頻可(kě)以清晰的看到,青瀾生物(wù)的微針由兩層構成,分(fēn)别是染色的針體(tǐ)部分(fēn)以及無色的基膜部分(fēn)。青瀾的第一個優勢,是能(néng)做到在室溫下,貼敷幾秒(miǎo)即可(kě)實現藥物(wù)針尖的向皮内遞送。第二個優勢在于,青瀾微針産(chǎn)品的生産(chǎn)過程隻有(yǒu)兩種溶液,分(fēn)别是針尖液和基膜液,制膜過程隻需要兩步。更難能(néng)可(kě)貴的是,視頻中(zhōng)的樣品并非實驗室制作(zuò),而是由青瀾生物(wù)的生産(chǎn)線(xiàn)制作(zuò)完成。青瀾生物(wù)一貫堅持,在嘗試某個新(xīn)工(gōng)藝前就充分(fēn)考慮到後續的可(kě)量化生産(chǎn)性,即研發的産(chǎn)品最終是否能(néng)在生産(chǎn)線(xiàn)實現穩定、高效的生産(chǎn)。
我們知道可(kě)溶解微針又(yòu)包含兩種生産(chǎn)工(gōng)藝,分(fēn)别是一體(tǐ)針工(gōng)藝(圖6)和分(fēn)層針工(gōng)藝(圖7),前者适用(yòng)于化藥,後者适用(yòng)于生物(wù)藥。
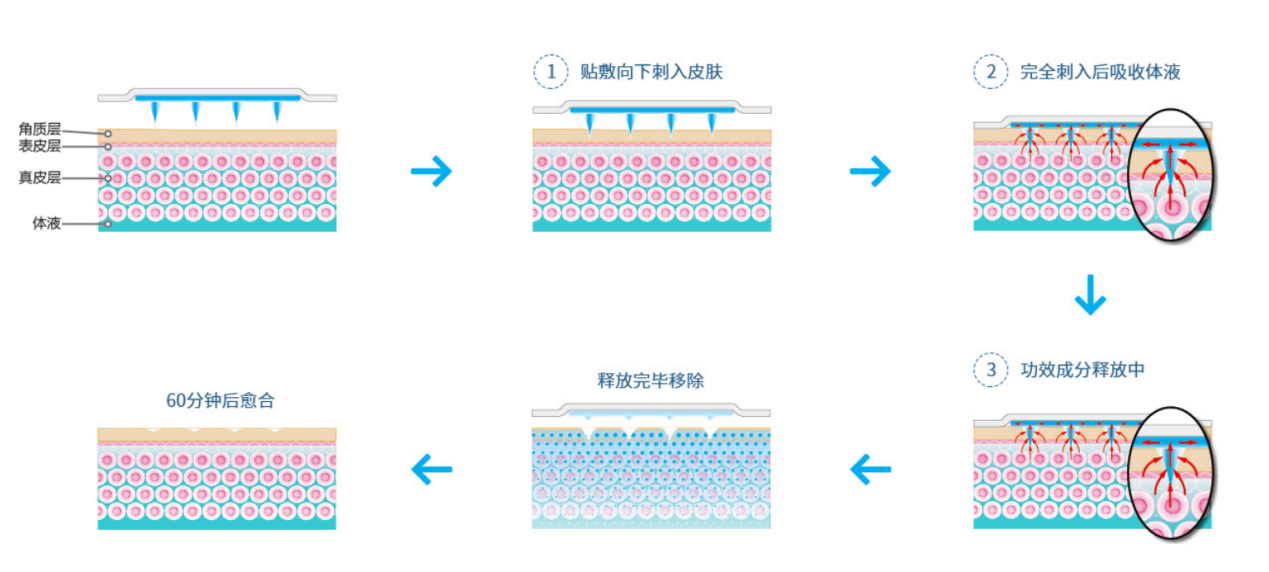

(圖6)
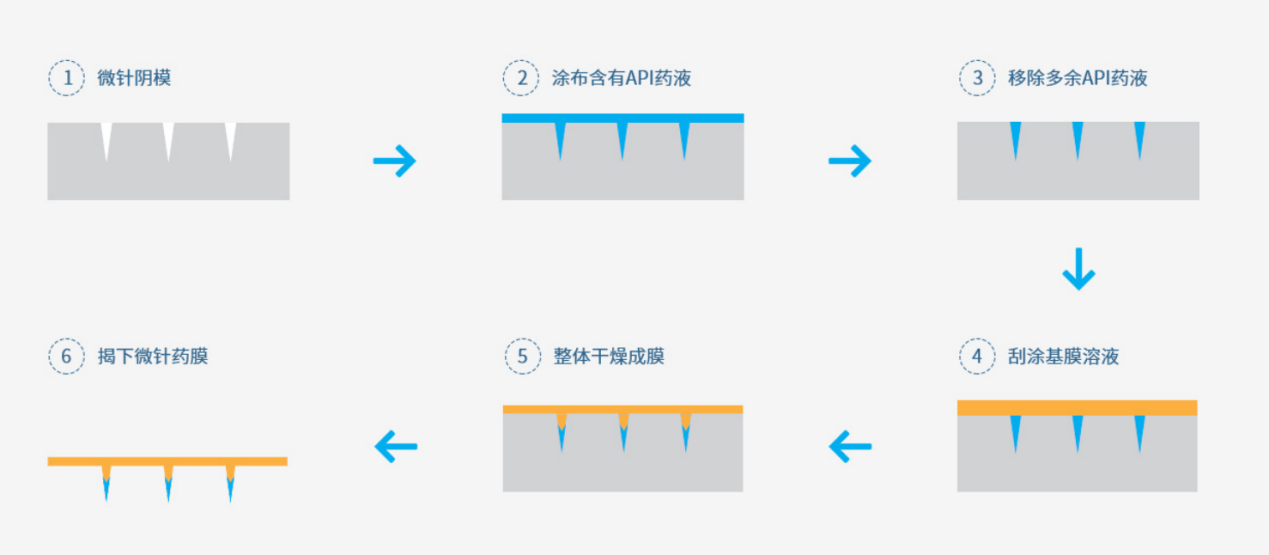

(圖7)
聶廣軍課題組的研究即采用(yòng)了分(fēn)層針工(gōng)藝。在全球微針産(chǎn)業化領域,能(néng)成功大規模量産(chǎn)一體(tǐ)針工(gōng)藝的公(gōng)司可(kě)謂寥寥,青瀾生物(wù)已經成功具(jù)備了分(fēn)層針的大規模量産(chǎn)能(néng)力。2021年9月23日,艾棣維欣董事長(cháng)兼首席科(kē)學(xué)家王賓教授帶領CMC團隊考察青瀾生物(wù)生産(chǎn)線(xiàn)(圖8),就工(gōng)藝的可(kě)靠性和産(chǎn)能(néng)情況進行了現場考察和确認。我們認為(wèi),産(chǎn)品的生産(chǎn)工(gōng)藝一定要可(kě)靠,産(chǎn)能(néng)一定要跟上,否則研究做得再漂亮,如果最終不能(néng)實現穩定量産(chǎn),那也隻有(yǒu)學(xué)術價值而無商(shāng)業價值。


(圖8)
鑒于與青瀾生物(wù)展開合作(zuò)的藥企越來越多(duō),2021年10月,青瀾生物(wù)在深圳銀星科(kē)技(jì )園投資建設了專門用(yòng)于微針藥物(wù)研發的GMP工(gōng)廠,計劃2021年12月31日之前投入使用(yòng)。
在産(chǎn)業化階段,在實驗室探索微針的工(gōng)藝已經變得沒有(yǒu)太多(duō)價值,因為(wèi)即使做出結果,無法固化工(gōng)藝條件,也無法具(jù)體(tǐ)知道實驗結果是在什麽樣的條件下做出。青瀾生物(wù)深圳茜坑工(gōng)廠不再參與藥物(wù)研發,專注生産(chǎn)化妝品等醫(yī)美類微針産(chǎn)品,從物(wù)理(lǐ)硬件上實現化妝品和藥物(wù)研發生産(chǎn)分(fēn)離。以DNA新(xīn)冠疫苗産(chǎn)能(néng)為(wèi)例,如果有(yǒu)需求,青瀾生物(wù)隻需要3000平方的廠房,就可(kě)以生産(chǎn)出足夠全球人民(mín)接種的疫苗微針貼。
三、法規問題
文(wén)獻研究中(zhōng)使用(yòng)了PEI納米顆粒包裹的DNA質(zhì)粒和非水溶性佐劑,成功地解決了透膜、溶酶體(tǐ)逃逸等的問題,PEI材料也是科(kē)學(xué)研究中(zhōng)基因藥物(wù)遞送常用(yòng)的轉染劑。然而,目前尚無一款使用(yòng)PEI作(zuò)為(wèi)輔料的藥物(wù)産(chǎn)品獲得監管部門的批準——PEI的細胞毒性是不可(kě)回避的現實風險。但在聶廣軍課題組的研究中(zhōng),也得到了非常明确的結論:無PEI納米顆粒包裹的裸DNA質(zhì)粒即使做成了微針,也沒有(yǒu)成功實現細胞轉染,也沒有(yǒu)檢測到有(yǒu)最終的抗原蛋白的表達,也就是說把裸DNA質(zhì)粒做成微針貼進行貼敷,是沒有(yǒu)免疫源性的,不能(néng)激起機體(tǐ)的免疫應答(dá)。
作(zuò)為(wèi)一個産(chǎn)業化企業,青瀾需要做可(kě)商(shāng)業化的産(chǎn)品。在面臨法規監管方面的難題和技(jì )術難題時,我們選擇了攻克技(jì )術難題,而不是挑戰監管。使用(yòng)一個不滿足監管要求的材料,可(kě)能(néng)會導緻我們的藥物(wù)開發在數年内原地踏步。
艾棣維欣與NASDAQ上市公(gōng)司INOVIO采用(yòng)電(diàn)轉儀作(zuò)為(wèi)DNA疫苗克服透膜和溶酶體(tǐ)逃逸的工(gōng)具(jù),并且商(shāng)品化了CELLECTRA電(diàn)轉儀,采用(yòng)電(diàn)脈沖的物(wù)理(lǐ)方式讓DNA質(zhì)粒進入細胞核。有(yǒu)了電(diàn)轉儀,青瀾生物(wù)在與艾棣維欣合作(zuò)開發過程中(zhōng),始終堅持遞送裸質(zhì)粒,不引入不符合法規的任何材料,并在動物(wù)實驗中(zhōng)獲得了較好的抗體(tǐ)滴度。
四、實驗數據穩定性
可(kě)溶解微針是一種藥物(wù)遞送方式,是一種劑型技(jì )術。2017年,FDA出了非強制性的微針類産(chǎn)品審評指南,并在2020年做了更新(xīn),将可(kě)溶解微針技(jì )術在審評原則上歸為(wèi)藥械組合,雖然我們堅持認為(wèi)可(kě)溶解微針本質(zhì)上是創新(xīn)劑型,但是對微針這樣颠覆性的技(jì )術,FDA出一個審評原則總比審評方式空缺要好,至少讓可(kě)溶解微針的研發和申報有(yǒu)了一個指導原則。歐洲、日本、中(zhōng)國(guó)的藥監部門應該都會參考這個審評指導原則。
可(kě)溶解微針既然是一種劑型,是藥物(wù)的承載和遞送方式,那麽可(kě)溶解微針産(chǎn)品的相關研究數據也應該是與藥品劑型研發有(yǒu)同等的要求。但目前行業大多(duō)企業關于可(kě)溶解微針的可(kě)靠性數據研究數據不夠穩定。部分(fēn)藥企的某款藥物(wù)采用(yòng)了微針劑型,所得到的研發數據雜亂無章,不要說拿(ná)去申報,可(kě)能(néng)自己内部都無法整理(lǐ)成确定的實驗結果。青瀾生物(wù)接觸過的某歐洲藥企,溝通完後認為(wèi)青瀾生物(wù)在微針方面确實談了一些之前未掌握的技(jì )術信息,但是不願意再次啓動微針項目,原因是其與美國(guó)某微針企業之前開展過一次微針藥物(wù)的研發合作(zuò),但是得到的研發數據很(hěn)不穩定,不能(néng)作(zuò)為(wèi)研發結果沉澱下來,最後不得不終止項目。
微針藥物(wù)研發的數據穩定性平行性,是阻礙微針行業産(chǎn)業化的重要因素,如果研發數據雜亂無章,那就說明這個微針技(jì )術不是穩定可(kě)靠的遞送方式,這是藥物(wù)這種特殊商(shāng)品所不能(néng)接受的。
我們反複強調可(kě)溶解微針技(jì )術是一個結果導向的技(jì )術,微針藥物(wù)研發數據的穩定性也隻能(néng)靠多(duō)批次的實驗結果來證明,而不能(néng)通過其他(tā)間接方式證明。
在我們與艾棣維欣合作(zuò)研究的9個月中(zhōng),青瀾生物(wù)負責微針制劑學(xué)開發、微針生産(chǎn)工(gōng)藝開發、微針質(zhì)量研究等方面的工(gōng)作(zuò),評價方面的所有(yǒu)工(gōng)作(zuò)由艾棣維欣完成,青瀾生物(wù)協助貼敷方法培訓。
在青瀾向艾棣維欣提供的若幹批次的樣品,不論每個批次的抗體(tǐ)滴度的絕對值高低,在批次内數據平行性都非常好,不論結果好壞,都非常好下清晰的結論。當收到艾棣維欣方面的結果反饋,青瀾生物(wù)在調整優化變量時,所得到的結果與所調整的變量剛性相關,研究邏輯随着研究的進展越發牢固。研究一路走來,逢山(shān)開路,逢水搭橋,有(yǒu)一些需要研究的基礎問題,整個文(wén)獻領域内都尚無人展開研究,我們都要去研究并找到相應的産(chǎn)業化解決之道。
困難道路需要結伴同行。在與艾棣維欣合作(zuò)2個月時,2021年4月雙方洽談展開戰略合作(zuò),由艾棣維欣戰略入股青瀾生物(wù),并于3個月後完成交割。這是雙方在技(jì )術、公(gōng)司文(wén)化兩方面的深度互信的結果。
基因藥物(wù)遞送幾乎是所有(yǒu)藥物(wù)遞送裏最難的,也是最麻煩的。青瀾生物(wù)有(yǒu)幸在啓動的第一個藥物(wù)項目就是DNA新(xīn)冠疫苗,在與艾棣維欣合作(zuò)的9個月裏,我們深入的與艾棣維欣的研發、質(zhì)量、法規注冊、CMC等各部門進行了多(duō)輪溝通,讓我們深刻的學(xué)習了滿足法規下的技(jì )術研發如何開展。
今年是青瀾生物(wù)的藥物(wù)研發年,下半年陸續有(yǒu)數家國(guó)内上市藥企與青瀾生物(wù)展開合作(zuò)。目前青瀾生物(wù)涉及的微針藥物(wù)涵蓋DNA疫苗、滅活疫苗、蛋白、多(duō)肽、水溶性化藥、非水溶性化藥等,我們的實驗室冰箱裏,存放了很(hěn)多(duō)藥企客戶郵寄過來的各種原料藥。路漫漫其修遠(yuǎn)兮,吾将上下而求索。青瀾生物(wù)的使命就是實現可(kě)溶解微針技(jì )術的産(chǎn)業化。


